BLOQUEO CAUDAL EN EL PACIENTE PEDIÁTRICO Dr. Javier Espinosa Franco Hospital Santa Fe, Ciudad de México. >]
El uso de técnicas de anestesia regional en el paciente pediátrico,data desde los primeros días de la anestesia regional. Brainbridge en 1901, y Gray en 1909 usaron la Cocaína y Estovaína para anestesia espinal en lactantes y niños. Campbell en 1933 reportó la primera serie de anestesia caudal en niños y posteriormente otros autores como Sievers (1936), Ruston (1957), Spiegel (1962) Fortuna (1967) para nombrar a los primeros (1). A pesar de esto dicha técnica no obtuvo generalizada y universal aplicación, teniendo como principal razón el inconveniente del uso asociado de anestesia general para poder realizar el procedimiento; sin embargo, con el paso de los años y múltiples estudios farmacocinéticos, farmacodinámicos, así como el advenimiento de nuevos medicamentos el bloqueo caudal es actualmente, la técnica de anestesia regional más utilizada (2, 3). En la ciudad de México, Distrito Federal, en el año 2000, de 101 anestesiólogos pediatras entrevistados, el 90% utilizan dicha técnica (comunicación personal).
Entre algunas de sus principales ventajas tenemos que esta técnica es capaz de ofrecer efecto anestésico satisfactorio con mínimas alteraciones fisiológicas; cuando se utiliza asociada a anestesia general disminuye las necesidades de anestésicos y acelera el despertar; ofrece un periodo postoperatorio inmediato libre de dolor permitiendo el pronto contacto del paciente con sus padres y reinicio de la vía oral, disminuyendo en forma muy importante el trauma psicológico para el paciente; además es posible la colocación de un catéter peridural cuando es necesario
prolongar el efecto analgésico postoperatorio (4)

INDICACIONES
1. Niños con historia de hipertermia maligna.
2. Pacientes que presenten enfermedades neuromusculares que tengan reducción de la reserva respiratoria o reflejos faríngeos disminuidos.
3. Pacientes prematuros con historia de apnea que sean sometidos a procedimientos quirúrgicos de abdomen, genitourinarios o de extremidades inferiores.
4. Pacientes con enfermedad crónica de vías aéreas incluyendo asma y fibrosis cística.
CONTRAINDICACIONES
Se consideran como contraindicaciones absolutas:
1. Falta de consentimiento paterno.
2. Infección en el sitio de la inyección.
3. Coagulopatía.
Como contraindicaciones relativas tenemos:
1. En sentido legal estricto se permite la realización de técnicas de anestesia regional, en contra de la voluntad de menores cuando se considera preferible y existe el consentimiento paterno; sin embargo, cuando el paciente es lo suficientemente grande como para lograr el diálogo (arbitrariamente de cinco
años en adelante) debería ser realizado previa discusión y aceptación del niño.
2. Estados convulsivos mal controlados.
3. Vía aérea difícil. Se presume que el empleo de cualquier técnica de anestesia regional implica la capacidad de controlar la vía aérea, sobre todo en caso de urgencia, como cuando existen reacciones tóxicas o complicaciones del procedimiento. En este sentido es necesario valorar detenidamente el tipo de dificultad de vía aérea, ya sea dificultad para ventilar o dificultad para intubar, así como el tipo de
procedimiento quirúrgico y la posición del paciente durante el transoperatorio, antes de tomar la decisión de realizar o no un bloqueo caudal.
4. Anomalías anatómicas en el sitio de inyección, como espina bífida.
5. Hipovolemia. Los casos de hipovolemia moderada pueden ser corregidos previos a la realización del bloqueo. Los estados de hipovolemia severa con riesgo de sangrado profuso es una contraindicación absoluta para la realización de bloqueo caudal.
6. Enfermedad neurológica. Los bloqueos de conducción pueden ser usados ventajosamente en muchos pacientes con enfermedad neurológica o desórdenes neuromusculares, incluyendo parálisis cerebral, miopatías y neuropatías estables o progresivas, debiéndose seleccionar juiciosamente cada paciente (5)
CONSIDERACIONES ANATOMICAS
El hueso sacro, está formado por la fusión de las cinco vértebras sacras, formando un hueso triangular, convexo por atrás, cóncavo por adelante, que se articula con la quinta vértebra lumbar por arriba y con el cóccix por abajo. El hiato sacro, es la fusión incompleta de la lamina de la quinta y habitualmente la
cuarta vértebras sacras, siendo una apertura en forma de U invertida, que presenta a los lados los cuernos sacros . Pueden existir variaciones en este hueso que son de importancia para el anestesiólogo, como es la extensión de la espina bífida, que puede incluir la tercera lámina hasta toda
la extensión del sacro, anormalidades de los cuernos sacro, hiato falso o ausencia del mismo siendo esta variable reportada hasta en el 7.7% de los casos, lo cual haría al bloqueo caudal teóricamente imposible en estos casos.
En su exterior el sacro presenta los forámenes sacros anteriores y posteriores por los cuales pasan los ramos primarios, los forámenes posteriores están prácticamente ocluidos por ligamentos, los forámenes anteriores que son más grandes son un sitio de escape de los anestésicos del espacio peridural.
CANAL SACRO Y SU CONTENIDO
El canal sacro es la continuación del canal espinal lumbar que finaliza a nivel del hiato sacro. Aquí encontramos las diferencias anatómicas más significativas con respecto a la edad. Al nacimiento la medula espinal finaliza a nivel de L3 y el saco dural a nivel de S3, en cambio en el adulto terminan a nivel de L1 y S2
respectivamente (4).
También encontramos los plexos sacros que, aunque en forma inconstante, pero con frecuencia se localizan a nivel del la parte anterior del canal. El resto del canal está lleno de grasa epidural, cuya consistencia cambia de una textura laxa en los niños a una textura más fibrosa, casi una red en los adultos, siendo esta la característica que permite predecir la difusión el anestésico en los niños (6)
SEDACIÓN TRANSQUIRURGICA
Ya que las concentraciones anestésicas que utilizamos en el paciente pediátrico no producen habitualmente bloqueo motor importante es posible que el paciente pueda moverse durante el transquirúrgico. Desde mi punto de vista es más difícil mantener "quieto, inmóvil" al paciente (enocasiones durante horas) que la realización técnica del bloqueo caudal. Una discusión concienzuda de
este tema ameritaría una charla, por lo que aquí solo mencionaré algunas
generalidades.
MEDICACION PREANESTESICA
Es importante el uso de una benzodiacepina, ya sea de corta o larga duración, ya que además de disminuir el consumo de otros hipnóticos, sus cualidades amnésicas, como en el caso del Midazolam, son muy útiles para disminuir el trauma psicológico del pequeño.
INDUCCIÓN
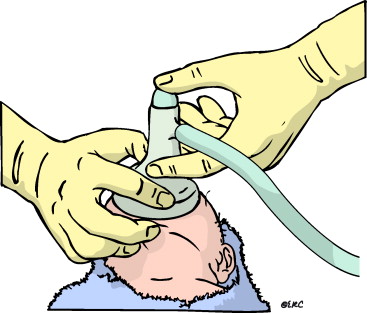
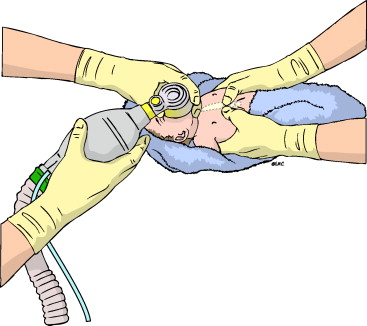
Puede ser endovenosa o inhalada. En el primer tipo puede ser disociativa, con previa atropinización. Se administra Ketamina (1-3 mg/kg) fraccionada; con este medicamento se tiene la ventaja de que la depresión respiratoria que se presenta es mínima cuando se administra lentamente. También puede usarse una combinación de Fentanilo-Propofol. Cuando se desea realizar la inducción inhalada se escoge un anestésico que produzca poca irritación de la vía aérea. El mantenimiento de la sedación puede realizarse con bolos de benzodiazepina o con infusión de propofol. Cuando sea necesario proteger la vía aérea o se halla planeado una técnica mixta puede realizarse la intubación orotraqueal o colocación de mascarilla laríngea antes o después de la realización de la punción, aunque prefiero realizarlo primero.
EJECUCIÓN DE LA PUNCIÓN
Posición del paciente: puede ser en la posición de Sims, es decir, decúbito lateral con las extremidades inferiores flexionadas la superior un poco más que la inferior , o en decúbito prono colocando una almohadilla por debajo de las crestas iliacas para la mejor exposición del hiato sacro. La elección de cual posición utilizar es personal, aunque se ha reportado que con volúmenes equivalentes la difusión del bloqueo es más alto en una a tres metámeras y se correlaciona mejor con el número de metámeras que se calculó bloquear, con la posición de Sims que con la genupectoral (7) Previa antisepsia de la reg lumbosacra, para la localización del hiato sacro, se puede trazar un triangulo equilátero cuyos vértices corresponden a las dos espinas iliacas posterosuperiores y al hiato mismo , o bien tocando con un dedo el cóccix se asciende hasta encontrar la depresión correspondiente al hiato.
Posteriormente para ubicar el sitio de punción se palpan los cuernos del sacro con los dedos pulgar e índice de la mano no dominante o bien colocando el dedo índice en el borde superior del hiato.
La introducción de la aguja que puede ser una mariposa No. 21 en los niños pequeños o bien una aguja hipodérmica o un catéter endovenoso en los mayores; se realiza con una angulación de entre 40 a 60 grados hasta experimentar el "clic" característico de penetrar el ligamento sacrocoxígeo. Posterior a esto se horizontaliza la aguja y se avanza dos o tres milímetros más en el espacio peridural . Esta
horizontalización se realiza para evitar puncionar hueso o el plexo venoso que, como ya se dijo, se encuentra en la parte anterior del canal. Después se comprueba pérdida de la resistencia administrando aire y teniendo desde aquí hasta el final de la punción un dedo sobre la piel del hiato para asegurar que no se está realizando una administración subcutánea.
Antes de administrar la dosis anestésica se aspira con suavidad para comprobar la inexistencia de sangre o líquido cefalorraquídeo; hay que recalcar, la aspiración de sangre puede ser falsa negativa porque las venas se colapsan fácilmente; además, cuando se realiza la punción con el paciente en decúbito prono el punto más alto corresponde al hiato sacro, por lo tanto no se obtiene retorno espontáneo de sangre por cuestiones hidráulicas. Más tarde se administra la dosis prueba del anestésico 0.1 ml/kg (8) que, de preferencia, debe contener epinefrina para detectar
administración intravenosa del mismo; si no existe cambio en la frecuencia cardiaca o tensión arterial,cambios en la onda T o en el segmento ST, se prosigue con la
administración del medicamento, que debe realizarse lentamente en uno o dos minutos, o bien un mililitro en 3 o 4 segundos (9)
Recordar que una administración muy rápida puede asociarse a una difusión proximal excesiva con riesgo de ocasionar trastornos respiratorios o aumentar
considerablemente la presión del espacio peri medular ocasionando perdida del
conocimiento o hipotensión arterial (10) La existencia de resistencia al administrar la dosis o el aumento de volumen de la región nos deben hacer sospechar la administración en sitio incorrecto.
BLOQUEO CAUDAL CONTINUO
Es posible la colocación de un catéter peridural del número 20 con una aguja de Tuohy pediátrica No.18, o un catéter para punción intravenosa cuando existe alguna indicación, como cirugía prolongada o necesidad de analgesia peridural postoperatoria, sin embargo es una práctica poco frecuente en nuestro medio debido al riesgo de contaminación. En el caso del catéter existen reportes de inserción de grades longitudes incluso hasta nivel torácico (11), práctica que no aconsejo por el riesgo de dañar la duramadre, la colocación intravascular o que el catéter se enrolle en sí mismo.
VOLUMEN DE INYECCIÓN
El volumen del anestésico administrado es otro de los factores que determina la altura metamérica alcanzada. Se han propuesto varios modelos matemáticos para determinar el volumen a administrar y la altura final del bloqueo sensitivo según la edad (12, 13, 14, 15) y el peso del paciente (13, 16); sin embargo, en la práctica clínica es más práctico seguir las siguientes recomendaciones (17, 18)
Volúmenes para anestesia caudal en pediatría:
1. Nivel lumbosacro: 0.5 mL/kg.
2. Toracolumbar: 1 mL/kg.
3. Medio torácico: 1.25 a 1.6 mL/kg.
DOSIS ANESTÉSICA
Las concentraciones plasmáticas consideradas como tóxicas en el adulto son de 3-7 ng/kg para Lidocaína y de 1.6 a 2 ng/mL para la Bupivacaína, siendo éstos valores aceptados para el paciente pediátrico. La utilización de soluciones con adrenalina permite reducir los picos plasmáticos para una dosis dada. En el niño las dosis máximas de Lidocaína simple son de 7 mg/kg y de 10 mg/kg para las soluciones con adrenalina, estos valores son de 2.5 a 4 mg/kg para la Bupivacaína, respectivamente
(19, 20) Las concentraciones de lidocaína utilizadas habitualmente en el paciente pediátrico son de 1%(0.8 en el neonato) y 0.25% para Bupivacaína. La adición de Fentanilo, 1-2 mcg/kg (21), mejora la calidad de la analgesia peridural de los anestésicos locales.
La Ropivacaína es un anestésico amida de larga duración, que en adultos muestra niveles plasmáticos venosos máximos tolerados superiores a los de Bupivacaína. A niveles venosos plasmáticos de 2.2 mcg/ml no se detectaron efectos colaterales. A dosis que producen depresión cardiovascular o síntomas neurológicos los cambios fueron menos pronunciados con ropivacaína que con Bupivacaína (22) La
experiencia clínica con el bloqueo caudal en pacientes pediátricos con este medicamento aún es limitada; se ha reportado el uso de volúmenes de 0.5 a 1 mL/kg, con concentraciones de 0.2 a 0.5% y dosis de 2 a 3.75 mg/kg (23, 24, 25, 26), obteniéndose anestesias satisfactorias y con concentraciones
plasmáticas por debajo de los 2 mcg/ml, sin evidencia clínica de toxicidad. Por lo que, considerando que la aplicación del bloqueo caudal, que generalmente es con dosis única y que la toxicidad de Ropivacaína es menor que la de Bupivacaína, son razones por las que su uso se puede preferir.
En mi experiencia, aunque es posible utilizar el bloqueo caudal para cirugías de abdomen superior, la empleo solo en neonatos y lactantes menores (hipertrofia pilórica, gastrostomías, etc.) Y, por otra parte, el volumen máximo que utilizo es 20-25 mL, que es un volumen que se utiliza en niños de 5 a 6 años, a los cuales es posible colocarles el bloqueo a nivel lumbar.
¿POR QUE FALLA LA TÉCNICA?
Existen dos razones por la que el bloqueo caudal no sea efectivo:
La primera es porque la dosis no se administre correctamente en el espacio peridural, y esto sucede cuando:
1. Se administra la dosis en tejido subcutáneo, lo que causa resistencia al administrar la dosis y aumento de volumen en el sitio de punción; y
2. Punción en un agujero sacro, en ocasiones al no identificar adecuadamente las referencias anatómicas se puede puncionar el tercero o cuarto agujeros sacros, lo que causará que se bloquee la raíz correspondiente.
La segunda causa de falla del bloqueo es porque la altura metamérica no es suficiente para la cirugía a realizar. Lo importante en este punto es reconocer el hecho y cambiar de técnica si es necesario, antes de recurrir al uso de la "polifarmacia" que puede ocasionar que el paciente se quede innecesariamente
"dormido", con lo cual se perderían algunas de las ventajas de la técnica.
INCIDENTES Y ACCIDENTES
1. Punción Vascular y Administración Intravascular. La perforación de una vena peridural es un accidente relativamente frecuente y sin consecuencias si se reconoce oportunamente, ya que hasta el 15% de las punciones son traumáticas, sobre todo si no se horizontaliza la aguja después de penetrar la membrana sacrococcígea; es importante realizar la aspiración suave antes y durante la administración del medicamento retirando la aguja si se obtiene sangre y volviendo a recolocarla en
espacio peridural, además de administrar la dosis prueba del anestésico con epinefrina para reconocer la localización intravascular de la aguja, de no hacerlo así ocurrirán las consecuencias tóxicas de la administración intravascular de anestésicos locales tales como convulsiones, trastornos del ritmo cardiaco, hemodinámicas y ventilatorios graves, que ameritarán su adecuado tratamiento.
2. Perforación de la Duramadre e Inyección Subaracnoidea. Una perforación dural puede
producirse por una anomalía anatómica, como cuando existe espina bífida. También se produce cuando la aguja ha sido avanzada excesivamente en el canal sacro. Su frecuencia es hasta del 2.5%. Si al
aspirar se obtiene líquido cefalorraquídeo se debe retirar la aguja y si se desea reintentarlo administrar la dosis muy lentamente después de la recolocación de la aguja y la verificación cuidadosa de su correcta colocación. Si pasa desapercibida la punción de la duramadre se pueden administrar grandes volúmenes de anestésicos locales en el espacio subaracnoideo, con la consecuente raquia masiva que puede ser de consecuencias catastróficas.
También se han reportado otros accidentes como: punción de médula ósea, inyecciones intraóseas(cuyos efectos son parecidos a la administración intravenosa directa) y el traspaso de la pared anterior del canal sacro con lesión de vísceras como el recto y los vasos pelvianos.
REFERENCIAS BIBLIOGRAFICAS
1. Cousins MJ. Bloqueos Nerviosos. Edición Española. Barcelona España. Ediciones Doyma S.A.; 1991.p690.
2. Dalens B,Hasnaoui A.Caudal Anestesia in Pediatric Surgery: Success Rate and Adverse effects in 750 consecutive patients. Anesth Analg 1989;68:83-9.
3. Giaufré E, Dalens B, Gombert, Epidemiology and Morbidity of Regional Anesthesia in Children: A oneyear prospective survey of the French-Language Society of Pediatric Anesthesiologists. Anesth Analg 1996;83:904-12.
4. Brown L. D. Regional Anesthesia and analgesia. Philadelphia, Pensylvania: W.B. Saunders Company; 1996. p 562.
5. Gregory G. Pediatric Anesthesia. 2nd. ed. Churchill Livigston; 1989. p. 647.
6. Dalens B. Anestesia Locorregional en Niños y Adolescentes. Barcelona: Masson-Williams & Wilkins España S.A.;1998. p. 180-182.
7. Mozo-Barrales AM. Influencia sobre Altura Metamérica de Bloqueo Alcanzado en Dos Posiciones durante el Bloqueo Caudal en Niños. Rev Mex Anest 1990;13:66-69.
8. Charles BB. Toxicity of local anesthetics in infants and children. The J. pediatr 1993;122: S14-S20.
9. McGrown RG. Caudal Analgesia in Children. Five hundred cases for procedures below the diaphragm. Anesthesia 1982;1:635-8.
10. Thorogood A, Casale F. Transient Loss of Consciousness after Caudal Injection. Anaesthesia 1985;40:1021-2.
11. Rasch D, Webster D, Pollard T, Gurkowaki M. Lumbar and Thoracic Epidural Anaesthesia for Postoperative Pain Relief in Infants and Children. Can J Anaest 1990;37:359-62.
12. Bromage PR. Ageing and Epidural Dose Requirements. Br J Anaesth 1969;41:1016-22.
13. Takasaki M, Dohi S, Kawabata Y, Takayashi T. Dosage of Lidocaine for Caudal Anestesia in Infants and Children. Anesthesiology 1977;47:527-9.
14. Hain WR. Anaesthetic Doses for Extradural Anaesthesia in Children. Br J Anaesth 1978:50;303.
15. Schulte-Steimberg O. Regional Anaesthesia for Children. Ann Chir Gynaecol 1984; 73: 158-65
16. Spiegel P. Caudal Anesthesia in Pediatric Surgery: a preliminary report. Anesth Analg 1962;41: 218-21.
17. Armitage EN. Regional Anaesthesia in Paediatrics. Clin Anaesthesiology 1985 3:553-68.
18. Melman E, Peñuelas J, Marrufo J. Regional Anesthesia in Children. Anesth Analg 1975;54:387-90.
19. Takasaki M. Blood Concentrations of Lidocaine, Mepivacaine and Bupivacaine during Caudal Analgesia in Children. Acta Anaesthesiol Scand 1984;28:211-4.
20. Yaster M, Maxwell L. Pediatric Regional Anesthesia. Anesthesiology 1989;70:324-3.
21. Berde CB, Sethna NF, De Jesus JM, Yemen TA, Mandell J. Continuous Epidural Bupivacaine-Fentanyl Infusions in Children Undergoing Urologic Surgery. Anesth Analg 1990;70:S22.
22. Knudsen K, Beckman-Suurkula M, Blomberg S, Sjövall J, Edvardsson N. Central Nervous and Cardiovascular Effects During IV Infusion of Ropivacaine, Bupivacaine and Placevo in Volunteers. Br J Anaesth 1997;78:507-14.
23. Koinig H, Creen CG, Glaser C, Marhofer P, Wildling E. The Dose-Response of Caudal Ropivacaine in Children. Anesthesiology 1999;90:1339-44.
24. Khalil S, Campos C, Farag AM, Vije H. Caudal Block in Children: Ropivacaine Compared with Bupivacaine. Anesthesiology 1999;91:1279-84.
25. Ala-Kokko TI, Partanen A, Karinen J. Pharmacokinetics of 0.2% Ropivacaine and 0.2% Bupivacaine following Caudal Blocks in Children. Acta Anaesthesiol Scand 2000;44:1099-102.
26. Wulf H, Peters C, Behnke H.The pharmacokinetics of caudal ropivacaine 0.2% in children. A study of infants aged less than 1 year and toddlers aged 1-5 years undergoing inguinal hernia reapir. Anesthesia 2000;55:757-760.