EUGENIO MARTÍNEZ HURTADO 1
SARA HERVILLA EZQUERRA 2
Aproximadamente un 10% de los recién nacidos (
RN) precisan algún tipo de ayuda para comenzar a respirar, y menos del 1% precisa manobras de resucitación (
LOE 4)
1,
2. Sin embargo, a pesar de que la gran mayoría de los RN no precisa ayuda, el gran volumen de nacimientos a nivel mundial hace que un gran número de niños precisen algún tipo de asistencia cardiorrespiratoria.
Continuamos revisando los cambios más importantes o los “
toques de atención” que el comité de expertos ha emitido en las nuevas recomendaciones para el Soporte Vital en el Neonato, tras revisar el documento internacional de consenso
3 y las guías publicadas tanto por el European Resuscitation Council (
ERC)
4 como por la American Heart Association (
AHA)
5, que incluyen:
- Retraso del pinzamiento del cordón.
- Control de la temperatura de los recién nacidos prematuros.
- Hipotermia terapéutica posreanimación.
- Aspiración.
- Monitorización de CO2 exhalado.
- Relación Compresión-Ventilación.
Las
recomendaciones se clasifican en I, IIA, IIB, III e Indeterminada y el nivel de evidencia científica que las respalda desde
LOE 1-5.
En caso de que el RN precise maniobras de resucitación, se realizará:
1. Estabilización inicial: calentar, limpiar la vía aérea si es necesario, secar, estimular.
2. Ventilación.
3. Compresiones torácicas.
4. Administración de epinefrina y/o expansores de volumen.
Entre el nacimiento, la realización de estas maniobras de estabilización inicial, la reevaluación de la situación del RN y el comienzo de la ventilación si es necesaria sólo pueden pasar 60 segundos (el denominado “minuto de oro”).
Se comenzarán las maniobras de reanimación si el RN no logra mantener una respiración adecuada o una frecuencia cardíaca mayor de 100 latidos por minuto (lpm).
Retraso del pinzamiento del cordón
Cada vez existen más evidencias del beneficio que supone retrasar el pinzamiento del cordón durante al menos 1

minuto en neonatos nacidos a término y pretérmino que no requieren reanimación. En RN deprimidos que requieran reanimación no hay actualmente suficiente evidencia para recomendar o rechazar una recomendación que retrase la ligadura del cordón.
Control de la temperatura de los RN prematuros
A los RN prematuros, con edad de gestación inferior a 28 semanas, se les debe cubrir hasta el cuello con una bolsa o sábana de plástico, sin secarles, inmediatamente después del nacimiento. La estabilización y demás cuidados se realizarán bajo una fuente de calor radiante. La cobertura se debe mantener hasta que se comprueba la temperatura después del ingreso en planta. La temperatura del paritorio debe ser de al menos 26ºC.
Hipotermia terapéutica posreanimación
Se recomienda proporcionar hipotermia terapéutica (de 33,5 °C a 34,5 °C) a los lactantes nacidos con 36 semanas o más de gestación con una encefalopatía hipóxico-isquémica de moderada a grave (
Clase IIa, LOE 1), puesto que en los estudios estos bebes presentaron una mortalidad significativamente menor y menos discapacidades de desarrollo neurológico en el seguimiento realizado a los 18 meses.
La hipotermia terapéutica debe administrarse con protocolos claramente definidos similares a los utilizados en los ensayos clínicos publicados y en centros con capacidad para proporcionar un cuidado multidisciplinario y un seguimiento longitudinal.
Manejo de la Vía Aérea
Una vez comenzada la administración de ventilación con presión positiva o de oxígeno adicional, deben evaluarse simultáneamente 3 características clínicas: la frecuencia cardíaca, la frecuencia respiratoria y el estado de oxigenación (idealmente determinado por pulsioximetría en lugar de la evaluación del color) (
Clase I, LOE 2).
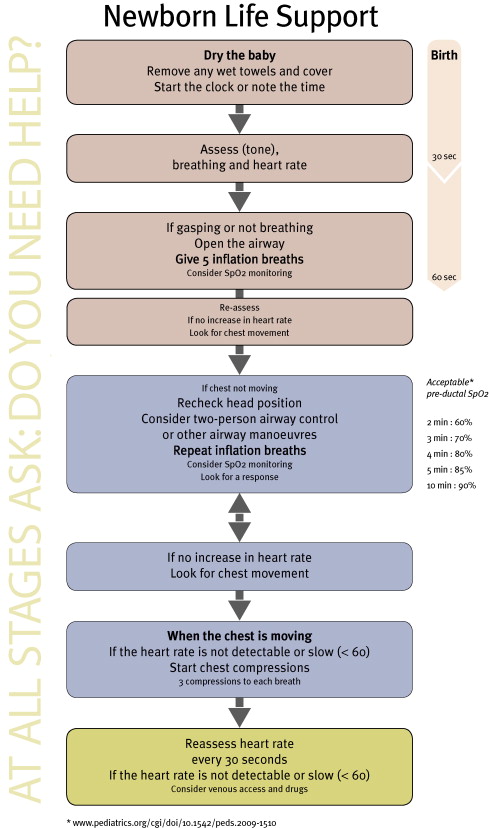 ERC 2.010 – Algoritmo de Reanimación en el Neonato
ERC 2.010 – Algoritmo de Reanimación en el Neonato
Administración de oxígeno adicional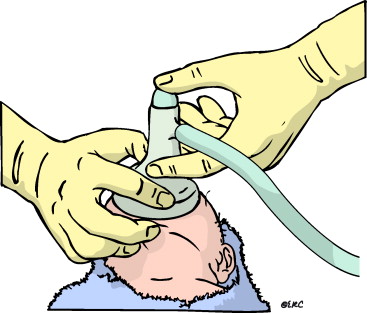
Los neonatos nacidos sanos y a término parten de una saturación de oxihemoglobina arterial inferior al 60%, y pueden tardar más de 10 minutos en alcanzar una saturación superior al 90%.
Debe utilizarse la pulsioximetría, con la sonda conectada a la extremidad superior derecha, para evaluar la necesidad de administrar O2 adicional. Se recomienda su uso cuando se anticipe la reanimación, cuando sea necesario mantener la ventilación con presión positiva (
VPP), si la cianosis persiste o si se administra O2 adicional (
Clase I, LOE 2)
En el caso de neonatos nacidos a término, es mejor comenzar la reanimación con aire mezclado con O2, en lugar de hacerlo con O2 al 100%, puesto que la hiperoxia puede ser tóxica, particularmente para el neonato prematuro (
Clase IIb, LOE 2). La administración de oxígeno adicional debe regularse mezclando O2 y aire, y usando una oximetría monitorizada en la extremidad superior derecha (es decir, la muñeca o la palma de la mano) a modo de guía para saber qué cantidad administrar (
Clase IIb, LOE 3).
Si no se dispone de la mezcla O2+aire se iniciará la reanimación con aire (
Clase IIb, LOE 2).
Si el RN está bradicárdico (FC < 60 lpm) tras 90 segundos de reanimación con una concentración baja de O2, ésta se aumentará hasta el 100% hasta que se recupere una frecuencia cardíaca normal (
Clase IIb, LOE 2).
Ventilación con Presión Positiva
Si el niño sigue en apnea o le cuesta respirar, o si la frecuencia cardíaca es < 100 lpm tras los pasos anteriores se debe comenzar con la VPP. La frecuencia respiratoria será de 40-60 respiraciones por minuto (
rpm) (
Clase IIb, LOE 3).
Aspiración
Si se aprecia líquido amniótico meconial mientras la cabeza se encuentre todavía en el periné de la madre no se recomienda aspirar la nariz y la boca del feto. La evidencia disponible no avala ni rechaza la aspiración endotraqueal rutinaria de lactantes deprimidos nacidos con el líquido amniótico teñido de meconio (
Clase IIb, LOE 3).
Si el recién nacido está hipotónico y en apnea, con obstrucción obvia de la respiración espontánea o necesidad de una VPP, es razonable visualizar orofaringe y aspirar (
Clase IIb, LOE 3), pudiendo ser útil la intubación traqueal y la aspiración si se dispone de personal entrenado en esta práctica. Sin embargo, si el intento de intubación es prolongado o sin éxito debe iniciarse la ventilación con mascarilla, sobre todo si hay bradicardia persistente.
Mascarillas Laríngeas
Se han mostrado eficaces para ventilar a RN que pesen más de 2000 gr. o tengan más de 34 semanas de gestación (
Clase IIb, LOE2), por lo que pueden usarse en aquellas situaciones en las que la mascarilla facial sea ineficaz y la intubación endotraqueal sea ineficaz o no sea posible (
Clase IIa, LOE 2).
No se ha comprobado su utilidad en casos de líquido amniótico meconial, durante las compresiones torácicas o para la administración de medicación intrataqueal.
AHA 2.010 – Algoritmo de Reanimación en el Neonato
Soporte Cardiocirculatorio
Relación Compresión-Ventilación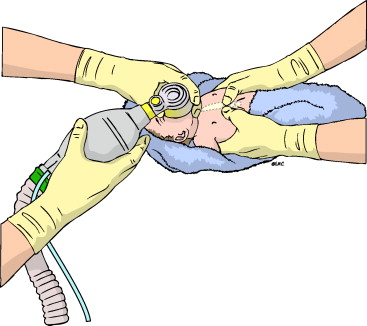
Se deben comenzar las compresiones cuando la frecuencia cardíaca sea menor de 60 lpm tras ventilar correctamente durante 30 sg. con O2 adicional (
Clase IIb, LOE 3).
El paro cardíaco neonatal suele producirse por asfixia, por lo que se ha mantenido la secuencia de reanimación A-B-C con una relación compresión-ventilación de 3:1, excepto cuando la etiología es claramente cardíaca, momento en el que se puede considerar una relación más alta de 15:2 (para 2 reanimadores) (
Clase IIb, LOE 3).
Medicación
Si la frecuencia cardíaca se mantiene < 60 lpm. a pesar de ventilar con O2 al 100% (con frecuencia tras intubación orotraqueal) y de las compresiones torácicas, puede considerarse el uso de epinefrina a una concentración de 1:10.000 (0,1 mg/mL), o expansores de volumen, o los 2 a la vez.
Epinefrina
Se recomienda administrar la epinefrina por vía intravenosa (
IV) (
Clase IIb, LOE 3), a dosis de 0,01 a 0,03 mg/kg.
Si no se ha logrado una vía iIV, y mientras se canaliza, puede iusarse el tubo endontraqueal (
TET) para administrar la epinefrina, teniendo en cuenta que se presisan dosis más altas para que sea efectiva (0,05 a 0,1 mg/kg) (
Clase IIb, LOE 3).
Expansores de volumen
Se administrarán expansores de volumen cuando se objetive o se sospeche pérdida de sangre y la frecuencia cardíaca del RN no responda a las maniobras de reanimación (
Clase IIb, LOE 3). Se recomienda una solución cristaloide isotónica o sangre en la reanimación inicial (
Clase IIb, LOE 3), a una dosis de 10 ml/kg que podrá repetirse. Se debe evitar la infusión rápida de volumen, puesto que está asociada a hemorragia intraventricular (
Clase IIb, LOE 3).
Glucosa
Los RN con bajos niveles de Glucosa tienen un mayor riesgo de daño cerebral y mal pronóstico tras un episodio de hipoxia, aunque no se han logrado establecer unos niveles de Glucosa que indiquen riesgo. Por tanto, tras la reanimación y tan pronto como sea posible, debe iniciarse una infusión de Glucosa IV para evitar la hipoglucemia (
Clase IIb, LOE 3).
Mantenimiento o interrupción de los esfuerzos de reanimación
En un recién nacido sin una frecuencia cardíaca detectable, que continúa siendo indetectable durante 10 minutos, es adecuado considerar la conveniencia de detener la reanimación (
Clase IIb, LOE 3).
A la hora de tomar la decisión de continuar los esfuerzos de reanimación más allá de 10 minutos sin frecuencia cardíaca, deben tenerse en cuenta factores como la etiología supuesta del paro, la gestación del neonato, la presencia o ausencia de complicaciones, el papel potencial de la hipotermia terapéutica y los sentimientos previos expresados por los padres en cuanto al riesgo aceptable de morbilidad. Cuando la gestación, el peso al nacer o las anomalías congénitas conllevan la práctica certeza de una muerte prematura y es probable que entre los pocos supervivientes la morbilidad sea inaceptablemente alta, no está indicada la reanimación.
Bibliografía
1.- Perlman JM, Risser R. Cardiopulmonary resuscitation in the delivery room. Associated clinical events. Arch Pediatr Adolesc Med. 1995;149(1):20-25. (
PubMed)
2.- Palme-Kilander C. Methods of resuscitation in low-Apgar-score newborn infants—a national survey. Acta Paediatr 1992;81:739–44. (
PubMed)
3.- Nolan JP et al. 2010 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science With Treatment Recommendations. Resuscitation 2010;81S:e1-e25. (
PubMed)
4.- Richmond S, Wyllie J. European Resuscitation Council Guidelines for Resuscitation 2010. Section 7. Resuscitation of babies at birth. Resuscitation 81 (2010) 1389–1399. (
PubMed) (
pdf completo) (
pdf Section 7).
5.- Kattwinkel J, Perlman JM, Aziz K, Colby C, Fairchild K, Gallagher J, Hazinski MF, Halamek LP, Kumar P, Little G, McGowan JE, Nightengale B, Ramirez MM, Ringer S, Simon WM, Weiner GM, Wyckoff M, Zaichkin J. Part 15: neonatal resuscitation: 2010 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Circulation. 2010 Nov 2;122(18 Suppl 3):S909-19. (
PubMed) (
pdf)
6.- Atherton N, Parsons SJ, Mansfield P. Attendance of paediatricians at elective Caesarean sections performed under regional anaesthesia: is it warranted? J Paediatr Child Health. 2006;42:332–336. (
PubMed)


 minuto en neonatos nacidos a término y pretérmino que no requieren reanimación. En RN deprimidos que requieran reanimación no hay actualmente suficiente evidencia para recomendar o rechazar una recomendación que retrase la ligadura del cordón.
minuto en neonatos nacidos a término y pretérmino que no requieren reanimación. En RN deprimidos que requieran reanimación no hay actualmente suficiente evidencia para recomendar o rechazar una recomendación que retrase la ligadura del cordón.
